
发布日期:2026-03-17浏览次数:239来源:蓝景科信
在植物科学领域,解析转录因子与DNA的互作机制是构建基因表达调控网络的核心,更是揭示植物生长发育、逆境适应等生命过程分子机制的关键。传统的ChIP-seq技术依赖高质量特异性抗体,这一局限性使非模式植物的研究面临巨大挑战。DAP-seq(DNA Affinity Purification Sequencing,DNA亲和纯化测序)技术的出现,为研究模式和非模式植物的转录调控研究提供了高效、精准的解决方案。本文将系统解析三种基于DAP-seq的转录调控研究思路,以期为相关领域的科研工作者提供有益的思路与启发。
一、技术介绍
(一)核心原理
DAP-seq通过体外表达出含有标签(如His、Halo标签)的目的蛋白,利用标签特异性配体纯化蛋白,再与基因组DNA片段孵育结合,然后富集与目的蛋白结合的DNA,经高通量测序及生物信息学分析,在全基因组范围内鉴定转录因子的结合位点(TFBS)。该技术无需目的蛋白特异性抗体,无需转基因材料,即可揭示转录因子与DNA的互作网络。
(二)蓝景科信DAP-seq技术路线图
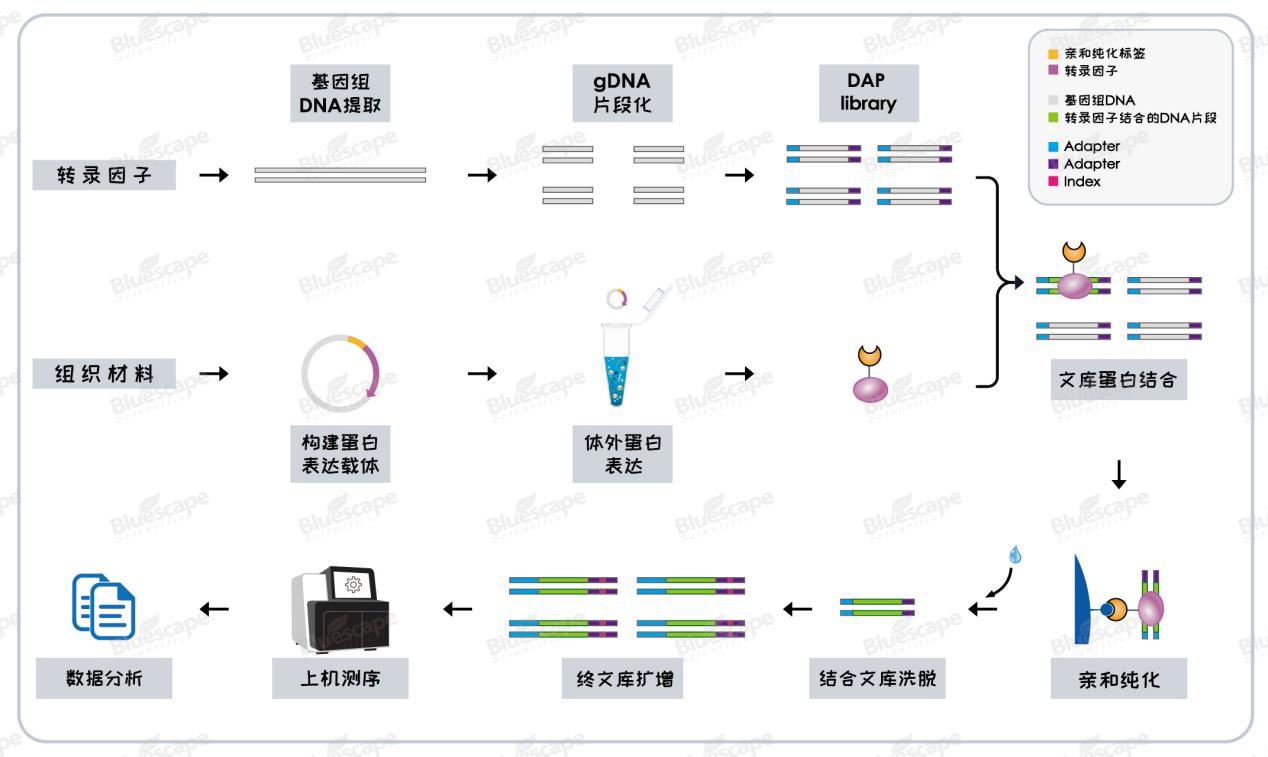
(三)技术优势
自2016年在《Cell》发表,2017年《Nature Protocols》发布标准化实验方法以来,DAP-seq迅速成为解析转录因子调控机制的关键技术。截至目前,蓝景科信使用该技术,已助力科学家在植物生长发育、逆境胁迫响应、果实发育、系统进化等多个研究方向取得突破,相关研究成果发表于Cell、Molecular Plant、Plant Biotechnology Journal、Plant Cell、PNAS、Plant Communications、New Phytologist、Plant Physiology等知名期刊。
二、三大实用研究思路与蓝景科信案例解析
(一)研究思路一:DAP-seq + 下游验证——精准锁定靶基因调控关系
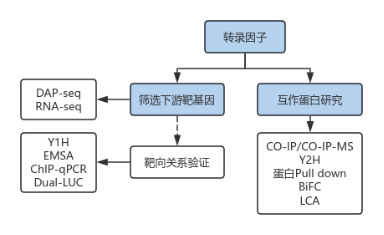
该思路以 “全基因组筛选 + 靶向验证” 为核心,先通过DAP-seq定位转录因子结合位点,结合RNA-seq筛选差异表达靶基因,再经体外与体内实验验证直接调控关系,是最基础且高效的研究框架。这是DAP-seq最基础且高效的研究框架,通过“全基因组筛选+靶向验证”的流程,明确转录因子与靶基因的直接调控关系。
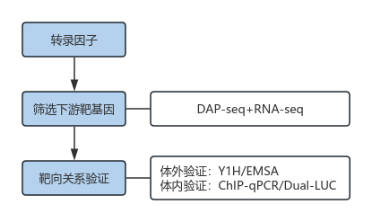
筛选阶段:利用DAP-seq定位转录因子的全基因组结合位点,结合RNA-seq筛选基因表达差异显著的靶标,通过联合分析缩小核心调控基因范围。
验证阶段:体外通过EMSA(凝胶迁移实验)、Y1H(酵母单杂)验证蛋白与DNA的特异性结合,体内通过ChIP-qPCR(染色质免疫共沉淀-实时荧光定量PCR)、Dual-LUC(双荧光素酶报告基因检测)确认调控关系。
案例1:紫花苜蓿MsMYB35调控花药发育研究

文章题目:Anther-specific expression of MsMYB35 transcription factor in alfalfa (Medicago sativa L.) and its crucial role in pollen development
发表期刊和时间:The Plant Journal(2025)
技术组合:DAP-seq、RNA-seq、Y1H、Dual-LUC
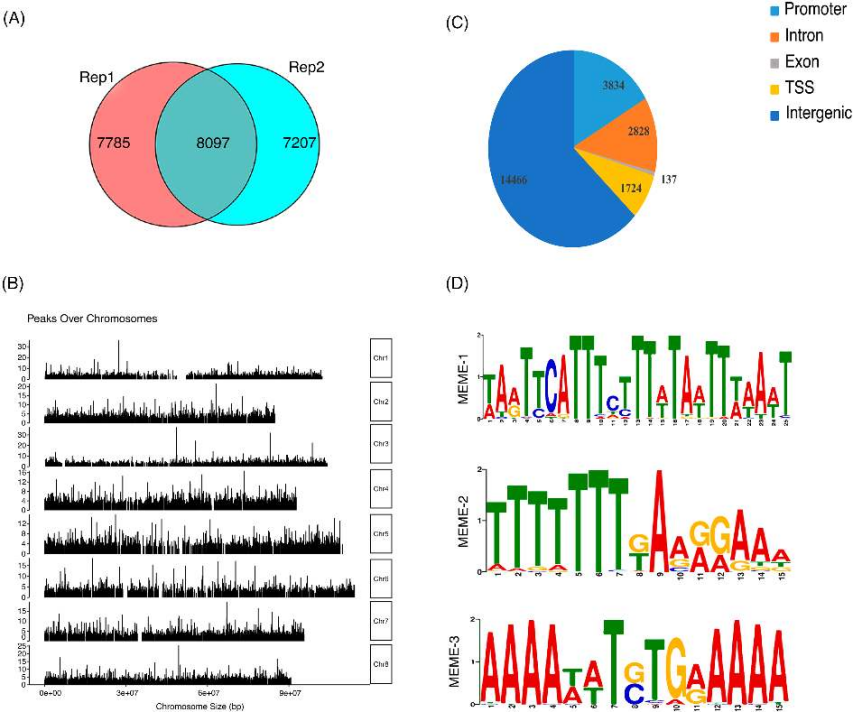
核心发现:DAP-seq鉴定出14,992个结合峰,其中8,097个高可靠性位点富集于基因间区(62.7%)和启动子区(16.6%),富集到AAAAA、TAAC、GA(A/G)三类保守基序,对应3,647个靶基因;联合RNA-seq筛选出467个直接调控基因,富集于苯丙烷代谢、茉莉酸(JA)合成、细胞壁重塑(如果胶裂解酶通路)等花药发育相关通路。酵母单杂交(Y1H)实验和双荧光素酶报告实验(Dual-LUC)证实MsMYB35可结合并激活MsJMT和MsPL基因表达,过表达MsMYB35促进花药发育,沉默则导致花粉不育,外源MeJA可恢复育性。
科学价值:本研究明确了MsMYB35的核心调控作用,为紫花苜蓿分子育种和杂交制种提供理论支撑。
案例2:软枣猕猴桃花青素调控机制研究

文章题目:Chromosome-level genome assembly assisting for dissecting mechanism of anthocyanin regulation in kiwifruit (Actinidia arguta)
发表期刊和时间:Molecular Horticulture(2025)
技术应用:DAP-seq、RNA-seq、EMSA、Y1H、ChIP-qPCR、Dual-LUC
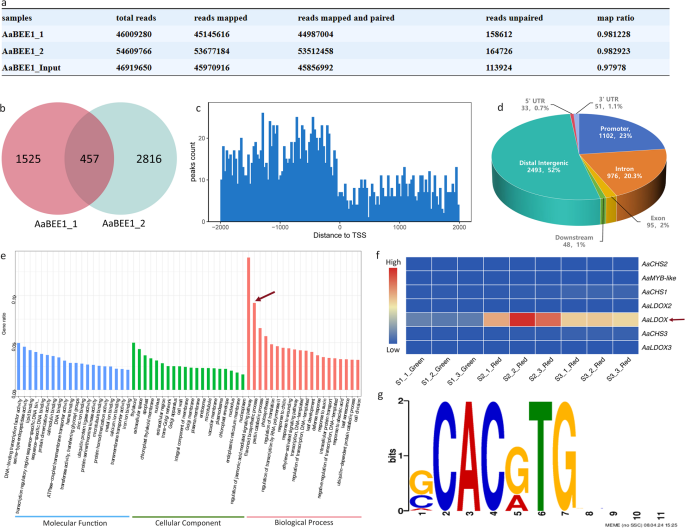
核心发现:组装首个全红软枣猕猴桃染色体水平基因组,通过对不同颜色的软枣猕猴桃品种进行RNA-seq分析,筛选出花青素抑制因子AaBEE1;DAP-seq鉴定AaBEE1在全基因组范围内的457个结合峰,靶基因显著富集于黄酮类生物合成通路,其中LDOX基因与果实颜色紧密相关。通过Y1H、EMSA、ChIP-qPCR和LUC等实验证实AaBEE1通过结合AaLDOX启动子的G-box区域抑制其表达,且AaLDOX启动子的29-bp indel 变异可影响基因表达效率。
研究思路二:DAP-seq + 互作蛋白——解析调控网络协同机制
在明确靶基因调控关系的基础上,结合蛋白互作研究可丰富调控网络的复杂性解析。该思路以DAP-seq和RNA-seq筛选靶基因为核心,整合Y2H、Co-IP、蛋白Pull-down、BiFC等蛋白互作研究技术,揭示转录因子与其他蛋白的协同作用模式,深化对调控机制的理解。
蛋白互作研究方法
酵母双杂交(Y2H)作为经典的蛋白互作研究方法,利用酵母转录因子的结构特征,通过观察酵母在营养缺陷培养基上的生长情况或显色活性判断蛋白互作。
免疫共沉淀(Co-IP)可在细胞内天然状态下捕获相互作用蛋白,通过WesternBlotting或质谱进行分析。
蛋白Pull down是体外研究蛋白质相互作用的经典方法,基于亲和层析原理,将诱饵蛋白与特定标签形成融合蛋白进行表达纯化,进而捕获并鉴定与之相互作用的蛋白。
双分子荧光互补(BiFC)则能直观判断目标蛋白在活细胞中的定位和相互作用。
荧光素酶互补实验(LCA)可通过检测发光信号强度评估蛋白间相互作用及强度。
案例3:拟南芥雄性育性调控网络解析

文章标题:A DELLA-ANAC106 reciprocal negative feedback circuit modulates gibberellin homeostasis to regulate male fertility in Arabidopsis
发表期刊和时间:New Phytologist(2025)
技术应用:DAP-seq、RNA-seq、EMSA、Dual-LUC、Y2H、CO-IP
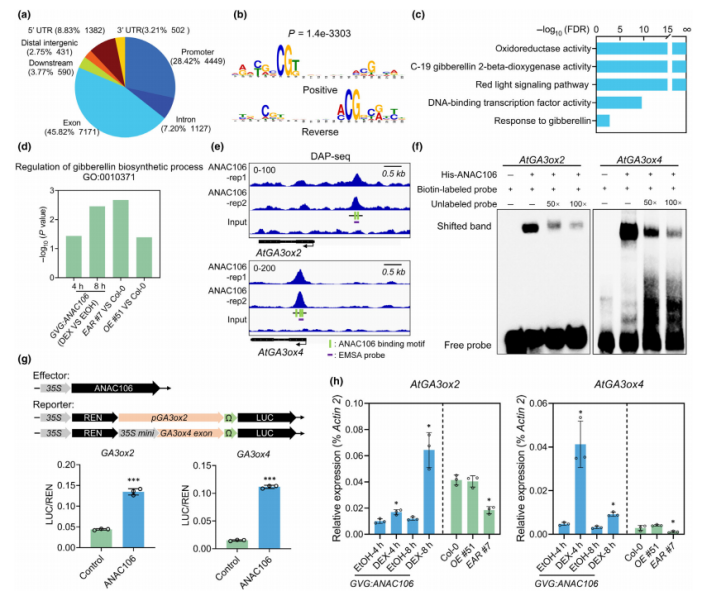
核心发现:本研究鉴定出NAC转录因子ANAC106,它在拟南芥幼嫩花药中高表达,其过表达或显性负抑制均会导致绒毡层降解异常(提前或延迟),进而引发雄性不育。借助DAP-seq结合RNA-seq数据分析,研究锁定ANAC106的直接靶标为GA合成基因GA3ox2/4和分解基因GA2ox1;EMSA与Dual-LUC实验进一步证实,ANAC106可激活GA3ox2/4的转录。通过Y2H和Co-IP显示ANAC106与4种DELLA蛋白(RGA、GAI等)互作,互作区域为ANAC106的N端,且DELLA蛋白以剂量依赖方式抑制ANAC106活性。二者形成双向负反馈回路,通过调控GA稳态维持雄性育性。
案例4:番茄果实成熟调控机制研究

文章标题:Protein phosphatase PP2C2 dephosphorylates transcription factor ZAT5 and modulates tomato fruit ripening
发表期刊和时间:Plant Physiology(2025)
技术应用:DAP-seq、RNA-seq、Y1H、EMSA、ChIP-qPCR、Dual-LUC、Y2H、CO-IP、BiFC、LCI、蛋白pull-down
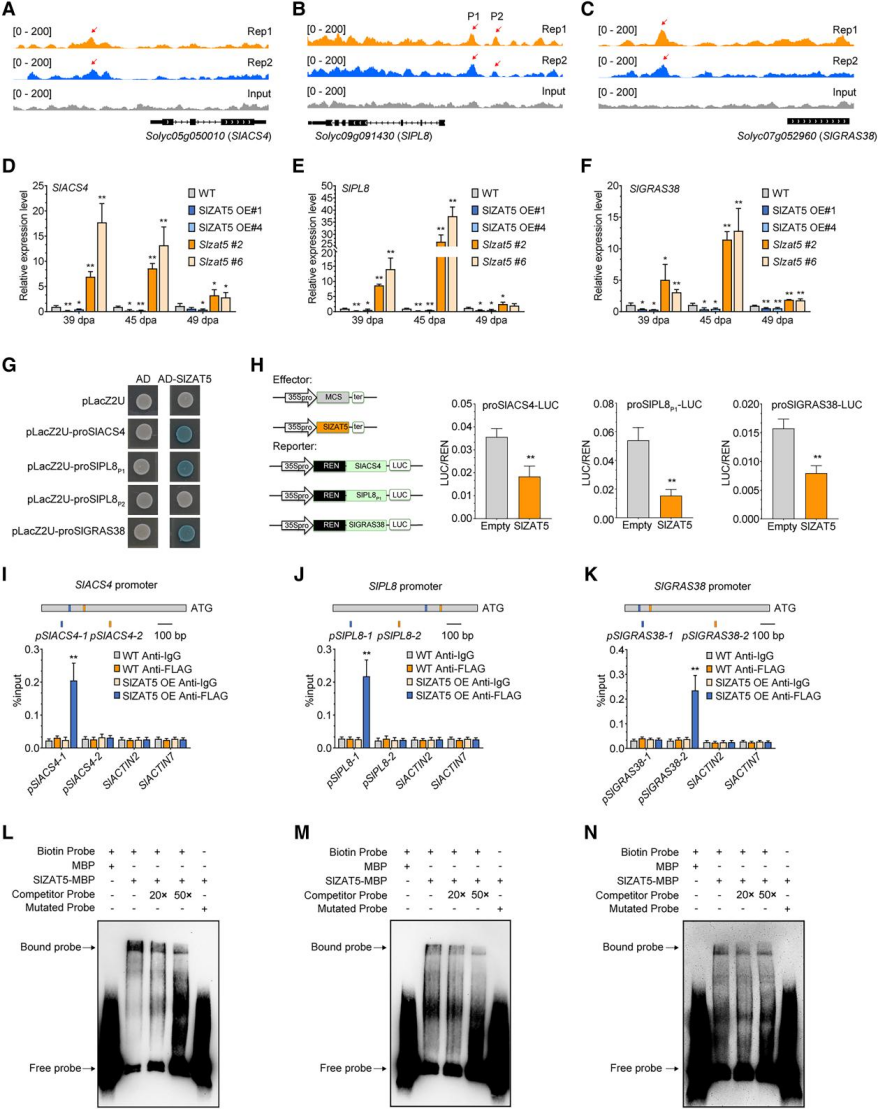
核心发现:SlZAT5负调控番茄果实成熟,DAP-seq结合RNA-seq鉴定到1511个成熟相关靶基因(含SlACS4、SlPL8、SlGRAS38等关键基因),经Y1H、Dual-LUC、ChIP-qPCR和EMSA实验证实SlZAT5可直接结合这些基因启动子并抑制其表达;。进一步通过Y2H筛选出SlZAT5的互作蛋白SlPP2C2,经BiFC、LCI、蛋白pull-down、Co-IP及亚细胞共定位实验确认二者在细胞核内相互作用,SlPP2C2通过去磷酸化SlZAT5的Ser-65位点,调控其转录抑制活性,进而影响乙烯合成与果实成熟。
研究思路三:DAP-seq+多组学联用——拓展研究深度与广度
将DAP-seq与ATAC-seq等多组学技术结合,从DNA结合、染色质可及性、基因表达等多维度解析调控机制,拓展研究的深度与广度,尤其适用于复杂性状调控网络的解析。
案例5:小麦氮高效利用与产量提升机制研究

文章题目:An incoherent feed-forward loop coordinates nitrate uptake and tillering in wheat
发表期刊和时间:Molecular Plant(2025)
技术应用:DAP-seq、ATAC-seq、RNA-seq、ChIP-qPCR、Y2H、Co-IP、BiFC、Y1H
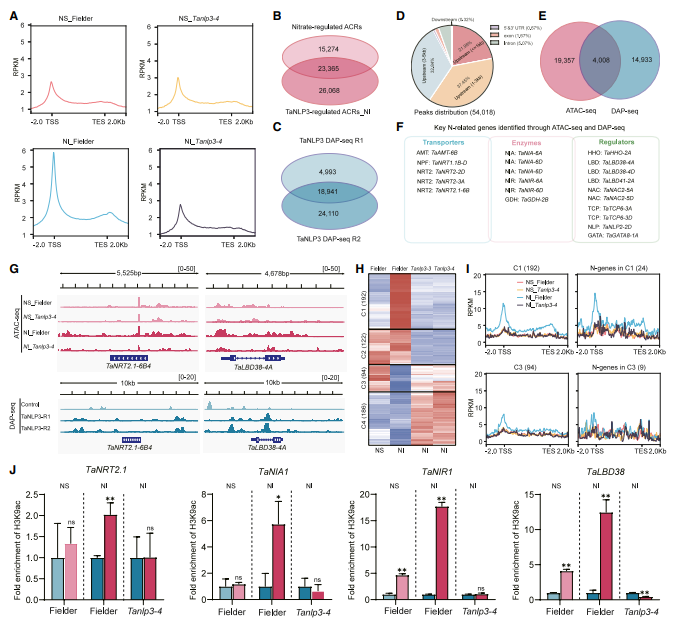
核心发现:TaNLP3是硝酸盐响应核心调控因子,与TaLBD38、TaNRT2.1构成非一致性前馈环路;Y2H证实TaNLP3与SWI/SNF染色质重塑复合物互作;ATAC-seq与DAP-seq联合分析显示,TaNLP3缺失显著降低硝酸盐诱导的染色质可及性,共调控4008个靶基因,参与氮吸收、同化等过程。同时鉴定的优异单倍型(TaNLP3-3BHap2等)为小麦高产高效育种提供遗传资源。
蓝景科信:转录调控研究的卓越合作伙伴
蓝景科信深耕功能基因组学领域,累计完成260+物种,4000+转录因子的实验项目,凭借高质量的服务,已助力合作客户在Cell,Science,Molecular Plant,Plant Biotechnology Journal,Journal of Advanced Research,Plant Cell,PNAS等数十知名期刊发表高质量研究成果。
我们的核心服务体系涵盖 DAP-seq及ATAC-seq、RNA-seq等组学技术,同时配套EMSA、Y1H、ChIP-qPCR、Dual-LUC等下游验证方案,并提供Y2H、Co-IP、蛋白Pull-down等全套蛋白互作服务。打造“组学检测—功能验证—互作分析” 一站式转录因子研究解决方案,全方位支撑科研工作高效推进!